غلظت یونها
غلظت یونها در محلول
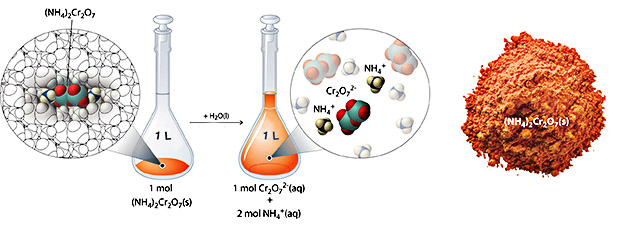
برای توضیح غلظت یونها در یک محلول، واکنشحل شدن آمونیوم دیکرومات را در آب نظر بگیرید:
(NH4)2Cr2O7(s)H2O(l)−−−−−−−→2NH+4(aq)+Cr2O2−7(aq)(NH4)2Cr2O7(s)→H2O(l)2NH4+(aq)+Cr2O72−(aq)
آمونیوم دیکرومات به عنوان ترکیبی یونی شناخته میشود که در هر مول از واحد فرمولی خود شامل یونهای Cr2O2−7Cr2O72− و NH+4NH4+ است. همانند دیگر ترکیبات یونی، این ترکیب نیز در دستهبندیالکترولیتهای قوی قرار میگیرد که به هنگام حل شدن در محلول آبی به یونهای تشکیل دهنده خود تفکیک میشود. در نتیجه، طبق واکنش بالا، هر مول آمونیوم دیکرومات به هنگام حل شدن در آب، یک مول Cr2O2−7Cr2O72− و ۲ مول NH+4NH4+ تولید میکند.
بنابراین، به هنگام محاسبات غلظت یونها در یک محلول باید واحد فرمولی آن و همچنین واکنش انحلال آنرا بدانیم. به طور مثال، به هنگام انحلال آمونیوم دیکرومات در آب، هر مول از آن به هنگام حل شدن، ۳ مول یون محلول در آب تولید میکند، یعنی اگر محلولی با غلظت 1.43M1.43M از آمونیوم دیکرومات داشته باشیم، غلظت کل یونهای محلول عبارتست از:
3×1.43 M=4.29 M
 یکی از آروزوهای قلبی من ایجاد یک فضای علمی و آموزشی همچنین مجالی برای تبادل و تضارب آرا و اندیشه ها بوده و هست . در ابتدای سال نوی شمسی بر آن شدم تا با خرید فضای بیشتر این وبلاک را به محلی برای اخذ و بسط ایده های همکاران دانش پژوهان و دانشجویان تبدیل نمایم . امید است با همت و همدلی شما سروران عزیز به این مهم نایل گردم .در صورت تمایل می توانم میز کار وبلاگ را در اختیار عزیزان معتمد قرار داده و یا از نظریات برجسته ی شما استفاده نمایم .
یکی از آروزوهای قلبی من ایجاد یک فضای علمی و آموزشی همچنین مجالی برای تبادل و تضارب آرا و اندیشه ها بوده و هست . در ابتدای سال نوی شمسی بر آن شدم تا با خرید فضای بیشتر این وبلاک را به محلی برای اخذ و بسط ایده های همکاران دانش پژوهان و دانشجویان تبدیل نمایم . امید است با همت و همدلی شما سروران عزیز به این مهم نایل گردم .در صورت تمایل می توانم میز کار وبلاگ را در اختیار عزیزان معتمد قرار داده و یا از نظریات برجسته ی شما استفاده نمایم .